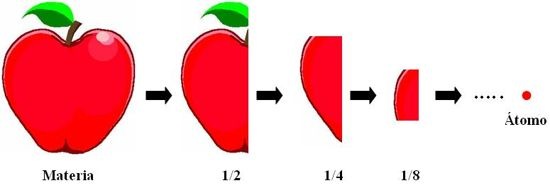
*Las primeras teorías surgieron en la Antigua Grecia, encabezadas por Demócrito y Leucipo, quienes postulaban que la materia se compone de partículas indivisibles llamadas átomos.

 Demócrito Leucipo
Demócrito Leucipo
*En 1803 el químico inglés John Dalton propone una nueva teoría sobre la constitución de la materia.
Según Dalton toda la materia se podía dividir en dos grandes grupos: los elementos y los compuestos.
Los elementos estarían constituidos por unidades fundamentales, que en honor a Demócrito, Dalton denominó átomos.
Los compuestos se constituirían de moléculas, cuya estructura viene dada por la unión de átomos en proporciones definidas y constantes. -La teoría de Dalton seguía considerando el hecho de que los átomos eran partículas indivisibles.
Dalton
Más tarde, en 1904 surge el primer modelo atómico, planteado por Thomson, explicando que el átomo era un "budín de pasas", donde la masa era positiva y en ella se incrustaban los electrones de carga negativa, éstos últimos descubiertos por él en 1897.
 En 1911, Rutherford introduce el modelo planetario, que es el más utilizado aún hoy en día.
En 1911, Rutherford introduce el modelo planetario, que es el más utilizado aún hoy en día.
Considera que el átomo se divide en:
· Un núcleo central, que contiene los protones y neutrones (y por tanto allí se concentra toda la carga positiva y casi toda la masa del átomo).
· Una corteza, formada por los electrones, que giran alrededor del núcleo en órbitas circulares, de forma similar a como los planetas giran alrededor del Sol.
*El modelo de Rutherford tuvo que ser abandonado, pues el movimiento de los electrones suponía una pérdida continua de energía, por lo tanto, el electrón terminaría describiendo órbitas en espiral, precipitándose finalmente hacia el núcleo.
El físico danés Niels Bohr en 1913, postula que los electrones giran a grandes velocidades alrededor del núcleo atómico. Los electrones se disponen en diversas órbitas circulares, las cuales determinan diferentes niveles de energía. El electrón puede acceder a un nivel de energía superior, para lo cual necesita "absorber" energía. Para volver a su nivel de energía original es necesario que el electrón emita la energía absorbida (por ejemplo en forma de radiación). Este modelo, si bien se ha perfeccionado con el tiempo, ha servido de base a la moderna física nuclear. 
El mecano-cuántico es el actual modelo, éste se expuso por primera vez en 1925 por Schrodinger y Heisenberg.
Sus aspectos y características:
Dualidad onda.partícula: la propuesta de Broglie; Todas las partículas materiales tienen propiedades ondulatorias y también que las partículas que están en movimiento lleva una onda asociada.
Principio de Indeterminación: La afirmación de Heisenberg con relación a que era imposible situar a un electrón dado en un punto exacto del espacio.